Год выпуска: 2009
Жанр: Кардиология
Формат: PDF
Качество: eBook (изначально компьютерное)
Описание:
Вашему вниманию предлагаются клинические рекомендации (руководства) «Национальные клинические рекомендации Всероссийского научного общества кардиологов», разработанные группами экспертов Всероссийского научного общества кардиологов и утвержденные на Российских Национальных конгрессах кардиологов. Клинические рекомендации - это периодически положения, помогающие практическому врачу и пациенту принять правильное решение, касающееся его здоровья, в специфических клинических условиях. Основу этих рекомендаций составляют клинические исследования и сделанный на их основе систематизированный обзор и мета-анализ. Клинические рекомендации обычно являются результатом длительной совместной работы специалистов, утверждаются профессиональными медицинскими обществами и предназначены врачам и организаторам здравоохранения, которые могут их использовать для подбора оптимальной терапии, разработки индикаторов качества и управления лечебно-диагностическим процессом, создания типовых табелей оснащения, непрерывного повышения квалификации врачей, формирования объемов медицинской помощи в рамках государственных гарантий.
Клинические рекомендации не имеют формальной юридической силы, а являются инструментом, помогающим врачам сделать оптимальный терапевтический выбор, однако они могут использоваться при решении вопросов о правильности лечения, в т.ч. в суде.
К сожалению, во всем мире, Россия не является исключением, существует большой разрыв между существующими рекомендациями и реальной клинической практикой. На то имеются различные причины:
- врачи не знают об их существовании, или не верят им;
- врачи считают, что они перегружены рекомендациями;
- врачи полагаются на личный опыт и на впечатления, что выбранный ими терапевтический подход является наилучшим;
- на решения врачей влияют экономические и социальные факторы.
Мы надеемся, что издание рекомендаций ВНОК в виде одной монографии облегчит их использование врачами в практической работе и будет способствовать повышению качества оказания помощи кардиологическим больным.
РАЗДЕЛ I
Диагностика и лечение артериальной гипертензии
Комитет экспертов
Общества
1.Введение
2. Определение
3. Классификация АГ
3.1. Определение степени повышения АД8
3.2. Факторы, влияющие на прогноз; оценка общего (суммарного) сердечно-сосудистого риска
3.3. Формулировка диагноза
4. Диагностика
4.1. Правила измерения АД
4.1.1. Способы измерения АД
4.1.2. Положение больного
4.1.3. Условия измерения АД
4.1.4. Оснащение
4.1.5. Кратность измерения
4.1.6. Техника измерения
4.1.7. Измерение АД в домашних условиях
4.1.8. Суточное мониторирование АД
4.1.9. Изолированная клиническая АГ
4.1.10. Изолированная амбулаторная АГ(ИААГ)
4.1.11. Центральное АД
4.2. Методы обследования
4.2.1. Сбор анамнеза
4.2.2. Физикальное обследование
4.2.3. Лабораторные и инструментальньи методы исследования
4.2.4. Исследование состояния органов-мишеней
4.2.5. Генетический анализ у больных АГ
5. Тактика ведения больных АГ
5.1. Цели терапии
5.2. Общие принципы ведения больных
5.3. Мероприятия по изменению ОЖ
5.4. Медикаментозная терапия
5.4.1. Выбор антигипертензивного препарата
5.4.2. Комбинированная терапия АГ
5.4.3. Сопутствующая терапия для коррек ции имеющихся ФР
6. Динамическое наблюдение
7. Особенности лечения АГ у отдельных групп больных
7.1. АГ у лиц пожилого возраста
7.2. АГ и МС
7.3. АГ и СД
7.4. АГ и ЦВБ
7.5. АГ и ИБС
7.6. АГ и ХСН
7.7. АГ при поражении почек
7.8. АГ у женщин
7.9. АГ в сочетании с патологией легких
7.10. АГ и СОАС
7.11. Рефрактерная АГ
7.12. Злокачественная АГ
8. Диагностика и лечение вторичных форм АГ
8.1. АГ, связанная с патологией почек
8.2. АГ при поражении почечных артерий
8.3. Феохромоцитома
8.4. Первичный альдостеронизм
8.5. Синдром и болезнь Иценко-Кушинга
8.6. Коарктация аорты
8.7. Лекарственная форма АГ
9. Неотложные состояния
9.1. Осложненный ГК
9.2. Неосложненный ГК
10. Показания к госпитализации
11. Партнерские отношения с пациентами
12. Заключение
13. Литература
Рабочая группа по подготовке текста рекомендаций
РАЗДЕЛ II
Диагностика и лечение стабильной стенокардии
Общества
1. Введение
2. Классы рекомендаций и уровни дока зательств
3. Определение и причины стенокардии
4. Эпидемиология и факторы риска
4.1. Эпидемиология
4.2. Естественное течение и прогноз
4.3. Факторы риска (ФР)
5. Диагностика стенокардии
5.1. Основные клинические признаки
5.2. Состояния, провоцирующие и усугуб ляющие ишемию миокарда
5.3. Физикальное обследование
5.5. Инструментальная диагностика
5.5.1. ЭКГ в покое
5.5.2. Рентгенография органов грудной клетки
5.5.3. ЭКГ пробы с ФН
5.5.4. Чреспищеводная предсердная элек трическая стимуляция (ЧПЭС)
5.5.5. Амбулаторное мониторирование ЭКГ
5.5.6. ЭхоКГ в покое
5.5.7. Стресс-ЭхоКГ
5.5.8. Перфузионная сцинтиграфия миокарда с нагрузкой
5.5.9. Мультиспиральная компьютерная томография (МСКТ) сердца и коронарных сосудов
5.6. Инвазивные методы изучения анатомии КА
5.6.1. КАГ
6. Классификация преходящей ишемии миокарда
6.1. Стабильная стенокардия
6.2. Вазоспастическая (вариантная) стено кардия
6.3. Безболевая (немая) ишемия миокарда
7. Дифференциальная диагностика синд рома боли в грудной клетке
8. Особенности диагностики стабильно стенокардии у отдельных групп больных и при сопутствующих заболеваниях
8.1. Стенокардия у молодых
8.2. Стенокардия у женщин ФР ИБС у женщин
8.3. Стенокардия у пожилых
8.4. Стенокардия при АГ
8.5. Стенокардия при СД
8.6. Кардиальный синдром X
9. Стратификация риска
9.1. Стратификация риска на основании клинических данных
9.2. Стратификация риска на основании стресс-тестов
9.3. Стратификация риска на основании КАГ
10. Лечение
10.1. Цели и тактика лечения
10.2. Основные аспекты немедикаментозного лечения стенокардии
10.3. Фармакологическое лечение
10.3.1. Лекарственные препараты, улучшающие прогноз у больных стенокардией
10.3.2. Медикаментозная терапия для купирования симптомов
10.3.3. Критерии эффективности лечения
10.3.4. Особые ситуации: синдром X и ва-зоспастическая стенокардия
10.4. Реваскуляризация миокарда
10.4.1. Коронарное шунтирование
10.4.2. Чрескожные вмешательства на коронарных артериях
11. Современные немедикаментозные технологии лечения стабильной стенокардии
11.1. Усиленная наружная контрапульса-ция (УНКП)
11.2. Ударно-волновая терапия сердца (УВТ)
11.3. Трансмиокардиальная лазерная терапия (ТМЛТ)
12. Оздоровление образа жизни и реабилитация больных стабильной стенокардией
13. Приложения
13.1.Литература
13.2. Список основных многоцентровых исследований
13.3. Основные лекарственные препараты для лечения стабильной стенокардии
РАЗДЕЛ III
Функциональное состояние почек и прогнозирование сердечно-сосудистого риска
Рабочая группа по подготовке текста рекомендаций
Состав комитета экспертов ВНОК по разработке рекомендаций
Общества
1. Введение
2. Основные определения
3. Методы оценки функции почек
3.1. Креатинин сыворотки
3.2. Скорость клубочковой фильтрации и клиренс креатинина
3.3. Экскреция белка с мочой
3.3.1. Методы определения экскреции альбумина с мочой
3.3.2. Диагностические критерии микроальбуминурии и протеинурии
4. Диагностические критерии и классификация хронической болезни почек
5. Скрининг пациентов для выявления нарушения функции почек
5.1. Алгоритм для определения нарушения функции почек
5.2. Диагностика повреждения почек
6. Ведение пациентов с хронической болезнью почек и мониторирование функции почек
6.1. Коррекция артериального давления и общие принципы ведения пациентов с хронической болезнью почек
6.2. Выявление и коррекция дислипидемии.
6.3. Диагностика и коррекция анемии
7. Функция почек в особых ситуациях
7.1. Артериальная гипертония
7.2. Метаболический синдром
7.3. Хроническая сердечная недостаточность
7.4. Острый коронарный синдром и инфаркт миокарда
8. Заключение
9. Приложения
10. Литература
РАЗДЕЛ IV
Диагностика и лечение хронической сердечной недостаточности
Рабочая группа по подготовке текста рекомендаций
Состав комитета экспертов ВНОК по разработке рекомендаций
Общества
I. Введение
11. Эпидемиология СН в Российской Федерации
III. Терминология, используемая при описании СН
IV. Определение ХСН
1. Принципы диагностики ХСН
1.1. Роль симптомов и объективных признаков в диагностике ХСН
1.2. Электрокардиография
1.3. Гематологический и биохимический анализы крови и общий анализ мочи
1.4. Эхокардиография
1.5. Магнитно-резонансная томография
1.6. Радиоизотопные методы
1.7. Оценка функции легких
1.8. Нагрузочные тесты
1.9. Рентгенография органов грудной клетки
1.10. Определение уровня натрий-урети-ческих пептидов
1.11. Оценка тяжести ХСН/ Классификация ХСН
1.12. Алгоритм постановки диагноза ХСН
2. Лечение ХСН
2.1. Цели при лечении ХСН
2.2. Профилактика ХСН
3. Немедикаментозное лечение ХСН
3.1. Диета больных с ХСН
3.2. Алкоголь
3.3. Режим физической активности
3.4. Методика проведения физических нагрузок в форме ходьбы
3.5. Режим. Общие рекомендации
3.6. Психологическая реабилитация и создание школ амбулаторного наблюдения для больных ХСН
3.7. Медико-социальная работа
4. Медикаментозное лечение ХСН. Общие принципы
5. Основные препараты для медикаментозного лечения ХСН
5.1. Ингибиторы АПФ
5.1.1 Побочные эффекты (требующие остановки лечения) осложняют применение иАПФ достаточно редко
5.1.2. Практические вопросы применения иАПФ при ХСН (дозы, тактика лечения, меры предосторожности)
5.2. Блокаторы в-адренергических рецепторов
5.3. Антагонисты альдостерона
5.4 Диуретические (мочегонные) средства в лечении ХСН
5.4.1. Общие вопросы дегидратационной терапии ХСН
5.5. Сердечные гликозиды
5.6. Антагонисты рецепторов к ангиотен-зину II
6. Дополнительные средства в лечении ХСН
6.1. Статины
6.2. Антитромботические средства в лечении ХСН (непрямые антикоагулянты)
7. Вспомогательные средства в лечении ХСН
7.1. Периферические вазодилататоры
7.2. Блокаторы медленных кальциевых каналов
7.3. Антиаритмические средства в лечении ХСН
7.4. Антиагреганты (в частности, аспирин) в лечении ХСН
7.5. Негликозидные инотропные средства в лечении ХСН
7.6. Метаболически активные препараты (цитопротекторы) при лечении ХСН
7.7 Средства, не рекомендованные к применению при ХСН
8. Медикаментозная терапия больных с ХСН и сохраненной систолической функцией ЛЖ или диастолической ХСН
9. Хирургические и электрофизиологические методы лечения ХСН
9.1. Электрофизиологические методы лечения ХСН
9.2. Хирургические и механические методы лечения ХСН
V. Приложение
Приложение 1. Классификация ХСН ОССН 2002 (с комментариями и приложениями)
Приложение 2.
Перечень исследований
VI. Литература
РАЗДЕЛ V
Диагностика и лечение больных острым инфарктом миокарда с подъемом сегмента ST ЭКГ
Рабочая группа по подготовке текста рекомендаций
Состав комитета экспертов ВНОК по разработке рекомендаций
Общество
1. Введение
2. Терминология OKOiST и OKiST
3. Некоторые звенья патогенеза OKdST (ИМ^Т)
4. Клиническая картина
4.1. Предынфарктный период. Нестабильная стенокардия
4.2. Классический (типичный) вариант ИМпБТ
4.3. Атипичные формы ИМпБТ
5. Диагностика ИМ^Т
5.1. Анамнез
5.2. Физикальное исследование
5.3. Клеточный состав крови и СОЭ
5.4. Повышение температуры тела
5.5. ЭКГ
5.6. Биохимические маркеры некроза миокарда
5.7. Рентгенография органов грудной клетки
5.8. УЗИ
5.9. Радионуклидные методы
5.10. Дифференциальная диагностика
5.11. Оценка размеров очага поражения
5.12. Необходимые и достаточные признаки для диагностики ИМ Критерии ОИМ
6. Общие принципы организации медицинской помощи больным ИМ^Т
6.1. БИК для коронарных больных
6.1.1. Расположение и планировка БИК
6.1.2. Оборудование БИК
6.1.3. Персонал БИК
6.1.4. Некоторые вопросы организации работы БИК
6.1.5. Длительность пребывания в БИК
7. Оценка тяжести состояния (прогноза) больного в начальном периоде заболевания
8. Лечение в начальном периоде заболевания
8.1. Обезболивание. Седативная терапия
8.2. Кислородотерапия
8.3. Органические нитраты
8.4. АСК
8.5. Клопидогрел
8.6. НФГ и НМГ
8.7. Другие антитромботические препараты
8.8. Блокаторы в-адренергических рецепторов
8.9. Ингибиторы РААС
8.10. Профилактика ФЖ
8.11. «Метаболическая» терапия и контроль уровня глюкозы в крови
8.12. Соли магния
8.13. Блокаторы кальциевых каналов
8.14. Физическая активность
8.15. Диета
8.16. Регуляция физиологических отправлений
9. Восстановление коронарной перфузии
9.1. Общая концепция
9.2. Значение фактора времени
9.3. ТЛТ. Показания, противопоказания
9.4. Тромболитические препараты. Схемы лечения
9.5. Сопутствующая терапия
9.6. Осложнения ТЛТ
9.7. Диагностика и оценка восстановления перфузии миокарда
9.8. Реперфузионный синдром. Феномен «по-reflow»
9.9. ТБА
9.10. Выбор метода реперфузионной терапии
9.11. Хирургическая реваскуляризация миокарда
10. Осложнения ИМ
10.1. Острая СН
10.1.1. Шок
10.1.2. Застой крови в малом круге кровообращения. Отек легких
10.1.3. Контроль показателей центральной гемодинамики
10.2. Лечение острой СН
10.2.1. Лечение шока
10.2.2. Лечение отека легких
10.3. Разрывы сердца
10.3.1. Разрыв МЖП
10.3.2. Инфаркт сосочковой мышцы; разрыв сосочковой мышцы
10.3.3. Разрыв наружной стенки ЛЖ (внешний разрыв сердца)
10.4. Острая аневризма ЛЖ
10.5. Артериальные ТЭ
10.6. ТЭЛА
10.7. Перикардит
10.8. Повторная ишемия миокарда. Ранняя постинфарктная стенокардия. Повторный ИМ
10.9. Нарушения ритма и проводимости
10.9.1. Наджелудочковые аритмии
10.9.2. Желудочковые аритмии
10.9.3. Брадиаритмии
10.10. ИМ ПЖ
11. Лечение в обычных палатах кардиологического отделения
11.1. Антиагреганты
11.2. Антикоагулянты
11.3. Блокаторы в-адренергических рецепторов
11.4. Органические нитраты
11.5. ИАПФ
11.6. Блокаторы рецепторов ангиотензина II
11.7. Блокаторы рецептора альдостерона
11.8. Статины
11.9. Сроки пребывания в стационаре
12. Оценка состояния больного перед выпиской из стационара
12.1. Определение функции ЛЖ. Выявление и оценка жизнеспособного миокарда
12.2. КАГ
12.3. Оценка и прогнозирование нарушений ритма и проводимости Желудочковые аритмии и ВСС
13. Лечение больных после выписки из стационара
13.1. Контроль АД
13.2. Физическая активность
13.3. Курение
13.4. Диета
13.5. Контроль веса
13.6. Воздействие на липидный профиль
13.7. Антиагреганты АСК
13.8. Антикоагулянты
13.9. Блокаторы в-адренергических рецепторов
13.10. Ингибиторы РААС
13.11. Лечение нарушений ритма сердца и профилактика ВСС
13.12. Лечение СД
13.13. Прочее медикаментозное лечение
14. Приложения
Приложение 1. Клиническая классификация типов ИМ
Приложение 2. Заболевания и состояния, затрудняющие ЭКГ диагностику ИМпБТ
Приложение 3. Причины повышения уровня сердечных тропонинов в крови при отсутствии очевидных проявлений ИБС
Приложение 4. Критерии инфаркта миокарда
Приложение 5. Лечение неосложненного ИМпБТ на догоспитальном этапе
Приложение 6. Формулы расчета клиренса креатинина и скорости клубочковой фильтрации
Приложение 7. Оценка прогноза больного ИМпБТ в ранние сроки заболевания
Приложение 8. Классификации тяжести кровотечений
Приложение 9. Степень коронарного кровотока по критериям TIMI
Приложение 10. Медикаментозное лечение ИМпБТ
Приложение 11. Правила перехода с антикоагулянтов прямого действия на антикоагулянты непрямого действия
Приложение 12. Начальная энергия электрического разряда при устранении аритмий, не связанных с остановкой кровообращения
Приложение 13. Вторичная профилактика ИМ
РАЗДЕЛ VI
4.2.4. Производные фиброевой кислоты (фибраты)
4.2.5. Никотиновая кислота
4.2.6. ш-З ПНЖК
4.2.7. Комбинированная терапия
4.2.8. Экстракорпоральные методы лечения
4.3. Особенности коррекции нарушений липидного обмена в отдельных группах больных
5. Заключение
6. Резюме российских рекомендаций «Диагностика и коррекция нарушений липидного обмена с целью профилактики и лечения атеросклероза». (Краткие рекомендации)
Последовательность диагностики и коррекции нарушений липидного обмена
10-летний риск смерти от ССЗ в популяциях с высоким риском ССЗ
Рабочая группа по подготовке текста рекомендаций
Состав комитета экспертов ВНОК по-раз-работке рекомендаций
Общества
РАЗДЕЛ VII
Диагностика и лечение метаболического синдрома
1. Введение
2. Факторы, влияющие на развитие МС
3. Определение МС
4. Диагностика МС
4.1. Критерии диагностики МС
4.2. Дополнительные критерии
4.3. Формулировка диагноза при МС
Диагностика и коррекция нарушений липидного обмена с целью профилактики и лечения атеросклероза
Состав комитета экспертов ВНОК по разработке рекомендаций
Общества
1. Введение
2. Основные нарушения липидного обмена и липидные ФР
2.1. Липидные ФР развития ССЗ и оптимальные значения липидных параметров
3. Нелипидные ФР развития ССЗ атеро-склеротического генеза
3.1. Категории риска
3.2. Оценка индивидуального риска смерти от ССЗ. Таблица SCORE
3.3. Скрининг ДЛП
4. Коррекция ФР и терапия ДЛП
4.1. Немедикаментозные меры профилактики атеросклероза
4.1.1. Диета
4.1.2. Коррекция веса
4.1.3. ФА
4.1.4. Прекращение курения
4.1.5. Употребление алкоголя
4.2. Медикаментозная терапия нарушений липидного обмена
4.2.1. Ингибиторы ГМГ-КоА редуктазы (статины)
4.2.2. Ингибитор абсорбции ХС в кишечнике (эзетимиб)
4.2.3. Секвестранты желчных кислот (ион-но-обменные смолы)
4.4. Примеры диагностических заключений
4.5. Диагностика МС на уровне первичного звена здравоохранения (в условиях городских, районных поликлиник)
4.6. Диагностика МС в условиях стационаров и специализированных клиник
4.7. Методы диагностики МС
4.8. Дифференциальная диагностика МС
5. Лечение МС
5.1. Основные принципы лечения МС
5.2. Немедикаментозное лечение ожирения
5.3. Лечение больных с ожирением и нарушениями дыхания во время сна
6. Медикаментозное лечение ожирения
6.1. Препараты, влияющие на ИР
6.2. Гиполипидемическая терапия МС
6.3. Антигипертензивная терапия
7. Комбинированная ашигипертензив-ная терапия у больных с МС
8. Алгоритм лечения больных с МС
9. Заключение
10. Литература
РАЗДЕЛ VIII
Диагностика и лечение легочной гипертензии
Рабочая группа по подготовке текста рекомендаций
Общества
1. Введение
2. Определение
3. Клиническая классификация ЛГ
3.1. Классификация врожденных системно-легочных шунтов
4. Патогенез ЛГ
5. Диагностика
5.1. Этапы диагностики ЛГ
6. Лечение ЛГ
6.1. Общие рекомендации
6.2. Медикаментозное лечение
6.3. Комбинированная терапия
6.4. Хирургическое лечение
7. Алгоритм лечения больных ЛГ
8. Приложение 1
9. Приложение 2
Шкала оценки одышки по Borg G 1982
РАЗДЕЛ IX
Лечение острого коронарного синдрома без стойкого подъема сегмента ST на ЭКГ
Подготовка текста рекомендаций
Состав комитета экспертов ВНОК по разработке рекомендаций
Общество
1. Введение
1.1. Некоторые определения
1.1.1. Соотношение понятий НС и ИМБП БТ. НС с повышенными уровнями СТр
2. Диагноз
2.1. Клиническая симптоматика
2.2. Физикальное обследование
2.3. ЭКГ
2.4. Биохимические маркеры повреждения миокарда
2.5. Оценка риска
2.5.1. ФР
3. Методы лечения
3.1. Антиишемические препараты
3.1.1. БАБ
3.1.2. Нитраты
3.1.3. АК
3.2. Антитромботические препараты. Антитромбины
3.2.1. Гепарины (НФГ и НМГ)
3.2.2. Прямые ингибиторы тромбина
3.2.3. Лечение геморрагических осложнений, связанных с терапией антитромбинами
3.3. Антитромботические препараты. Антитромбоцитарные средства
3.3.1. Аспирин (ацетилсалициловая кислота)
3.3.2. Антагонисты рецепторов к АДФ: тие-нопиридины
3.3.3. Блокаторы ГП Ilb/IIIa рецепторов тромбоцитов
3.4. Непрямые антикоагулянты при ОКС
3.5. Фибринолитическое (тромболитичес-кое) лечение
3.6. Коронарная реваскуляризация
3.6.1. КАГ
3.6.2. 4KB. Стенты
3.6.3. КШ
3.6.4. Показания к 4KB и хирургическим вмешательствам
3.6.5. Сравнение эффективности инвазив-ного и медикаментозного методов лечения
4. Стратегия лечения больных с ОКС
4.1. Первичная оценка больного
4.2. Больные с признаками острой окклюзии крупной КА
4.3. Больные с подозрением на ОКСБП БТ
4.3.1. Применение гепарина
4.3.2. Больные с высоким непосредственным риском смерти или развития ИМ по результатам начального наблюдения (8-12 часов)
4.3.3. Больные с низким риском смерти или развития ИМ в ближайшее время
4.4. Ведение больных после стабилизации состояния
5. Примерная последовательность действий при ведении больных ОКСБП ST
5.1. Первый контакт с врачом (участковым, кардиологом поликлиники)
5.2. Врач скорой помощи
5.3. Приемный покой больницы
5.3.1. Больницы без кардиологического БИТ или имеющие возможности для экстренного лечения больных в приемном покое
5.3.2. Больницы с кардиологическим БИТ
5.4. БИТ (при его отсутствии отделение, в котором осуществляется лечение)
5.4.1. Учреждения с хирургической службой или возможностью выполнения 4KB
5.5. Кардиологическое отделение после перевода из БИТ
6. Приложение
7. Литература
РАЗДЕЛ X
Диагностика и лечение острой сердечной недостаточности
Рабочая группа по подготовке текста рекомендаций
Состав комитета экспертов ВНОК по разработке рекомендаций
1. Введение
2. Эпидемиология и этиология ОСН
3. Определение и клиническая классификация ОСН
3.1. Клинические варианты ОСН (таблица 2)
3.2. Клинические синдромы при ОСН и основные способы лечения
4. Патофизиология ОСН
5. Диагностика ОСН
5.1. Оценка клинического состояния
5.2. ЭКГ
5.3. Рентгенография грудной клетки
5.4. Лабораторные исследования
5.5. ЭхоКГ
5.6. Другие диагностические методы
6. Цели лечения ОСН
6.1. Организация лечения ОСН
7. Мониторирование состояния больного с ОСН
7.1. Неинвазивное мониторирование
7.2. Инвазивное мониторирование
7.2.1. Катетеризация артерии
7.2.2. Катетеризация центральной вены
7.2.3. КЛА
8. Лечение ОСН
8.1. Общие подходы
8.2. Оксигенотерапия и респираторная поддержка
8.2.1. Оксигенотерапия
8.2.2. Дыхательная поддержка без эндотрахеальной интубации (неинвазивная вентиляция легких)
8.2.3. Дыхательная поддержка с эндотрахеальной интубацией
9. Медикаментозное лечение
9.1. Морфин
9.2. Вазодилататоры
9.2.1. Нитраты
9.2.2. Нитропруссид натрия
9.2.3. Незиритнд
9.2.4. АК
9.3. ИАПФ
9.4. Диуретики
9.5. БАБ
9.6. Инотропные средства
9.6.1. Допамин
9.6.2. Добутамин
9.6.3. ИФДЭ
9.6.4. Левосимендан
9.6.5. Вазопрессорные средства
9.6.6. Сердечные гликозиды
9.7. Антикоагулянты
9.8. Хирургическое лечение
9.9. Механические способы поддержки кровообращения
9.9.1. ВАКП
9.9.2. Средства поддержки желудочков сердца
9.10. Трансплантация сердца
10. Особенности лечения ОСН в зависимости от причины декомпенсации
10.1. ИБС
10.2. Патология клапанного аппарата сердца
10.3. Тромбоз искусственного клапана сердца
10.4. Расслаивающая аневризма аорты
10.5. Тампонада сердца
10.6. АГ
10.7. Почечная недостаточность
10.8. Заболевания легких и бронхооб-струкция
10.9. Нарушения ритма сердца
10.9.1. Брадиаритмии
10.9.2. Наджелудочковые тахиаритмии
10.9.3. Желудочковые аритмии
11. Тактика ведения больного с ОСН: итоговые рекомендации
РАЗДЕЛ XI
Диагностика и лечение фибрилляции предсердий
Рабочая группа по подготовке текста рекомендаций
Состав комитета экспертов ВНОК по разработке рекомендаций
Общества
1. Введение
2. Определение
3. Эпидемиология и прогноз
3.2. Заболеваемость
3.3. Прогноз
4. Классификация
5. Патофизиологические механизмы ФП
5.1. Патология предсердий у больных с ФП
5.2. Механизмы развития ФП
5.3. Электрическое ремоделирование предсердий
5.4. АВ проведение
5.5. Гемодинамические последствия ФП
5.6. Тромбоэмболии
6. Ассоциированные состояния и клинические проявления
6.1. Острые причины ФП
6.2. ФП без органической патологии сердца
6.3. ФП, связанная с органическим заболеванием миокарда
6.4. Нейрогенная ФП
6.5. Клиническая симптоматика
7. Принципы диагностики ФП
8. Лечение
8.1. Кардиоверсия
8.1.1. Фармакологическая кардиоверсия
8.1.2. Электрическая кардиоверсия
8.1.3. Рекомендации по фармакологической или электрической кардиоверсии ФП
8.2. Поддержание синусового ритма
8.2.1. Предикторы рецидивов ФП и фармакотерапия для их профилактики
8.2.2. Общий подход к антиаритмической терапии
8.2.3. Выбор антиаритмических препаратов у больных с некоторыми ССЗ, синдромами и их осложнениями
8.2.4. Рекомендации по фармакологической терапии для поддержания синусового ритма
8.3. Нефармакологические методы лечения ФП
8.4. Контроль 4ЖС при ФП
8.4.1. Рекомендации по контролю 4ЖС у больных с ФП
9. Профилактика тромбоэмболических осложнений
9.1. Стратегия АКТ или ААТ для профилактики ИИ и тромбоэмболии
9.1.1. Рекомендации по проведению АКТ или ААТ у больных с ФП
9.2. Восстановление синусового ритма
9.2.1. Рекомендации по АКТ и ААТ для профилактики ИИ и тромбоэмболии у пациентов с ФП, подвергающихся кардиоверсии
10. Отдельные заболевания
10.1. Послеоперационная ФП
10.1.1. Рекомендации по профилактике и лечению послеоперационной ФП
10.2. ОИМ
10.2.1. Рекомендации по лечению пациентов с ФП и ОИМ
10.3.WPW синдром
10.3.1. Рекомендации по лечению ФП и синдрома предвозбуждения желудочков
10.4. Гипертиреоз
10.4.1. Рекомендации по лечению ФП у больных с гипертиреозом
10.5. Беременность
10.5.1. Рекомендации по лечению ФП во время беременности
10.6. ГКМП
10.6.1. Рекомендации по лечению ФП у больных с ГКМП
10.7. Заболевания легких
10.7.1. Рекомендации по лечению ФП у больных с заболеваниями легких
11. Предлагаемые стратегии лечения - обзор алгоритмов лечения ФП
11.1. Впервые выявленная ФП (рисунок 4)
11.2. Рецидивирующая пароксизмальная ФП (рисунок 5, 6)
11.3. Рецидивирующая персистирующая ФП (рисунок 6,7)
11.4. Постоянная форма ФП (рисунок 7)
В настоящее время, по данным ВОЗ, около 250 миллионов человек в мире страдают хронической обструктивной болезнью легких (ХОБЛ). Это второе по распространенности неинфекционное заболевание по общемировой статистике. Заболеваемость ХОБЛ прогрессивно растет, и хроническая обструктивная болезнь легких является единственной причиной смерти с увеличением количества регистрируемых случаев . По прогнозам ВОЗ ХОБЛ станет третьей наиболее распространенной причиной смерти после инсульта и инфаркта миокарда к 2030 году . Наиболее часто встречающимися коморбидными состояниями при ХОБЛ являются артериальная гипертензия (АГ) (28%), сахарный диабет (14%), ишемическая болезнь сердца (10%) .
Приоритеты в изучении коморбидной сердечно-сосудистой и легочной патологии принадлежат отечественной терапевтической школе. Так, в 1954 году российский терапевт академик А. Л. Мясников выявил наклонность к повышению АД у больных эмфиземой легких и предположил ведущую роль в развитии гипертензивных реакций гипоксии головного мозга. Он писал: «В подобных условиях легче возникают, при действии психоэмоциональных факторов, соответствующие нарушения высшей нервной деятельности, которые ведут в ряде случаев к развитию гипертонии». Н. М. Мухарлямов в 1966 году отметил, что у 20-25% больных хроническими неспецифическими заболеваниями легких (ХНЗЛ) диагностируется АГ, связь которой с состоянием бронхиальной проходимости позволяет выделить ее в качестве самостоятельной симптоматической «пульмогенной» гипертонии. В генезе этой формы АГ Н. М. Мухарлямов предполагал участие гипоксии и гиперкапнии, нарушения роли легких в метаболизме биологически активных веществ (катехоламинов, серотонина, гистамина, кининов, ангиотензина II), которые являются вазоактивными агентами . В свою очередь В. Ф. Жданов и соавт. отмечали связь развития системной АГ с бронхообструкцией при участии гипоксии, гиперкапнии, нарушений легочного газообмена и гемодинамики малого круга кровообращения у больных ХНЗЛ, что подтверждается и более поздними исследованиями . В дальнейшем отечественные исследователи в целом ряде работ изучили патогенетические особенности АГ и клинико-функциональные характеристики АГ у больных ХОБЛ, а также подходы к терапии этой коморбидной патологии .
Однако до настоящего времени не существует доказательной базы эффективности антигипертензивной терапии и влияния на «суррогатные» и «жесткие» конечные точки у больных с сочетанной патологией АГ и ХОБЛ. Современные международные рандомизированные исследования в основном решают вопросы сравнения эффективности различных классов препаратов или их комбинаций. Возможности использования результатов данных исследований в реальной клинической практике зачастую ограничены, так как в список критериев исключения попадает большое количество больных АГ с сочетанной патологией, в том числе и ХОБЛ. С другой стороны, пульмонологические протоколы ведения больных с ХОБЛ не учитывают сочетанную кардиологическую патологию. Так, в европейских рекомендациях по ведению АГ (ESC/ESH 2007 — Европейское общество кардиологов (European Society of Cardiology — ESC) и Европейское общество по изучению гипертензии (The European Society of Hypertension, ESH)) вообще не выделяется такого клинического варианта АГ — сочетание с ХОБЛ . В национальных клинических рекомендациях в разделе «АГ в сочетании с патологией легких» обсуждаются особенности ведения АГ у больных с ХОБЛ и бронхиальной астмой, проблемы подбора антигипертензивных препаратов, предпочтительные терапевтические стратегии .
Не вызывает сомнения, что в лечении АГ при ХОБЛ оправдано назначение препаратов, не только эффективно снижающих АД, но и отвечающих ряду требований:
- адекватный контроль АД в ночные и ранние утренние часы;
- совместимость препаратов с базисными средствами лечения ХОБЛ;
- отсутствие эффектов, ухудшающих вентиляцию легких, бронхореактивность и усугубляющих гипоксемию;
- положительное влияние на гемодинамику малого круга кровообращения;
- выраженные кардио- и вазопротективные эффекты;
- отсутствие влияния на фармакодинамику антигипертензивных препаратов в условиях гипоксии.
Также необходимо, чтобы выбранный препарат оказывал влияние на патогенетические механизмы формирования АГ при ХОБЛ.
В основе развития АГ при ХОБЛ лежит раннее формирование эндотелиальной дисфункции в малом и большом круге кровообращения, повышение симпатической активности с дисбалансом синтеза катехоламинов, нарушение роли легких в метаболизме вазоактивных веществ, оксидативный стресс, хроническое системное воспаление, дисбаланс в ренин-ангиотензин-альдостероновой системе (РААС) . Имеются немногочисленные работы, подтверждающие роль компонентов РААС в патогенезе сердечно-сосудистых изменений у больных ХОБЛ . Активность ангиотензин-превращающего фермента (АПФ) увеличивается при гипоксии, что, возможно, играет немаловажную роль в увеличении степени системной гипертонии . Повышение функции РААС возможно как при непосредственном воздействии гипоксии, так и опосредованно, через активацию симпатоадреналовой системы.
Проблемы применения ингибиторов АПФ (ИАПФ) у больных с бронхообструктивным синдромом неоднократно обсуждались. И связаны они, прежде всего, с накоплением бронхоирритантов (брадикинин, субстанция Р, оксид азота) и появлением или усугублением кашля с возможным усилением бронхообструктивного синдрома. По данным клинических исследований частота этого побочного эффекта достигает 10-20%, причем среди больных без сопутствующей патологии . Появление брадикининового кашля у больных ХОБЛ может ошибочно расцениваться как обострение ХОБЛ и приводить к неоправданному изменению лечебной тактики: усилению противовоспалительной и бронходилатирующей терапии, что, в свою очередь, ведет к усугублению течения АГ, микроциркуляторным расстройствам и ухудшению качества жизни больных.
Блокаторы АТ 1 -ангиотензиновых рецепторов (БАР) в отличие от ИАПФ не влияют на активность других нейрогуморальных систем, с которыми связывают такие характерные для ИАПФ побочные эффекты, как сухой кашель и ангионевротический отек, при этом сохраняя плейотропные эффекты, характерные для блокады РААС (антиоксидантные эффекты, эндотелийрегулирующие свойства). Большей селективностью и специфичностью блокады РААС объясняют лучшую переносимость БАР, по сравнению с ИАПФ. Частота побочных эффектов при лечении БАР такая же, как при назначении плацебо. У пациентов с нарушенной бронхиальной проходимостью не было отмечено препарат-индуцированного кашля, что дает основания рассматривать БАР как препараты выбора в данной группе, что подтверждено в национальных рекомендациях Всероссийского научного общества кардиологов по ведению АГ (ВНОК, 2010) .
Однако в одной из работ на фоне применения лозартана было отмечено индуцирование бронхоспазма и появление кашля у пациентов с АГ. Среди предположительных механизмов этого побочного эффекта обсуждалось повышение освобождения бронхоирританта оксида азота . В другом же исследовании лозартан ингибировал метахолин-индуцированный бронхоспазм и значительно уменьшил редукцию объема формированного выдоха за первую секунду (ОФВ 1) .
Таким образом, влияние БАР на функцию легких описано в небольшом количестве местных исследований, которых недостаточно для однозначного заявления о тактике применения препаратов этой фармакологической группы у пациентов с сочетанием АГ и ХОБЛ в связи с небольшим количеством наблюдений и отсутствием ослепления исследований. Таким образом, теоретические предпосылки благоприятного действия блокады негативных влияний АТII дают основание для дальнейших исследований влияния данной группы препаратов не только при изолированной АГ, но и ее сочетании с другими патологиями, в том числе ХОБЛ.
Целью нашей работы явилась оценка эффективности и переносимости антагониста рецепторов ангиотензина II — валсартана (Нортиван®) в дозе 80-160 мг в сутки у больных АГ 1-2 степени и ХОБЛ II-IV стадии.
Материалы и методы исследования. Дизайн исследования — местное, открытое, несравнительное исследование по изучению эффективности и безопасности препарата Нортиван® у больных АГ в сочетании с ХОБЛ. Нами обследовано 18 пациентов с ХОБЛ II-IV стадии (the Global initiative for chronic Obstructive Lung Disease, GOLD 2011) в период ремиссии, страдающий АГ I и II степени, определяемой в соответствии с общепринятой классификацией уровней АД (ВНОК, 2010). Средний возраст больных составил 53,5 ± 4,6 года.
Критериями исключения из исследования являлось наличие у пациентов осложнений АГ, ишемической болезни сердца, декомпенсированного хронического легочного сердца, эндокринных заболеваний, требующих медикаментозной коррекции, патологии почек, хронической сердечной недостаточности, пероральной стероидной терапии более 10 дней за последние 6 месяцев до включения в исследование, онкологических заболеваний и любых других состояний, которые могли бы помешать интерпретации и оценке результатов исследования. Пациенты, не получавшие ранее антигипертензивного лечения, включались в исследование сразу, а остальные проходили отмывочный период в течение 2 недель.
В качестве антигипертензивной терапии на протяжении 24 недель пациенты получали препарат Нортиван®. Эффективность терапии контролировалась с помощью суточного мониторирования артериального давления (СМАД). Выбор в качестве критериев эффективности терапии параметров СМАД связан с литературными данными и собственными наблюдениями о преобладании у пациентов с АГ и ХОБЛ суточных профилей АД с отсутствием снижения или повышением АД в ночной период, когда офисные цифры АД в меньшей степени отражают эффективность проводимой антигипертензивной терапии. Начальная дозировка составила 80 мг/сут. При недостаточном гипотензивном эффекте на 4-й неделе лечения доза препарата удваивалась. Базисная терапия ХОБЛ не менялась на протяжении всего времени исследования и включала антихолинергические препараты (ипратропия бромид, тиотропия бромид), бета2-адреномиметик (фенотерол) или их комбинацию.
Исходно и через 24 недели лечения проводилось полное лабораторное обследование: клинический анализ крови, биохимический анализ крови. Также исследовалась толщина комплекса интима-медиа (КИМ) сонных артерий, ЭКГ. Критерием безопасности проводимой терапии послужила оценка показателей функции внешнего дыхания, суточной пульсоксиметрии. СМАД проводилось с использованием портативных мониторов АВРМ-03 и АВРМ-04. Суточная пульсоксиметрия проводилась с использованием пульсоксиметра MIROxi. При суточной пульсоксиметрии анализировались следующие параметры: Ср%SpO 2 — средний уровень сатурации за сутки; Мин%SpO 2 — минимальное значение сатурации за сутки; Макс%SpO 2 — максимальное значение сатурации за сутки; индекс десатурации (1/ч) — среднее количество эпизодов десатурации за час; максимальная продолжительность (c) — максимальная продолжительность десатурации. Вентиляционная функция легких оценивалась на бодиплетизмографе волюметрического типа Master Lab методами спирографии с компьютерным расчетом показателей. Критерием безопасности терапии были данные спирометрии и суточной пульсоксиметрии до назначения препарата и в процессе терапии.
Анализ данных проводился с помощью статистического пакета программ SPSS 15.0. При сравнении количественных признаков в параллельных группах использовался критерий Стьюдента.
Результаты и обсуждение
Все больные по данным СМАД на фоне лечения достигли целевых цифр АД. Увеличение дозы препарата до 160 мг/сут потребовалось 50% пациентов. Побочных эффектов в процессе терапии зарегистрировано не было.
Под влиянием терапии произошло статистически значимое снижение как среднесуточных показателей систолического артериального давления (САД) и диастолического артериального давления (ДАД), так и показателей АД в дневной и ночной периоды (табл. 1). При анализе суточного профиля АД до терапии обращало на себя внимание преобладание пациентов с повышением или отсутствием снижения АД в ночном периоде (night-peaker — 31%, non-dipper — 50%, dipper — 19%), что связано с усугублением бронхиальной обструкции в ночные часы с активацией нейрогуморальных систем (симпатико-адреналовой и РААС) и повышением АД. В процессе терапии произошла полная коррекция типа night-peaker с увеличением количества пациентов с физиологическим ночным снижением АД (dipper) до 62%.
В наше исследование вошли пациенты со значительными обструктивными нарушениями в целом по группе (ОФВ 1 < 60%). В процессе лечения существенной динамики данных спирометрии не получено, что доказывает безопасность и хорошую переносимость изучаемого препарата у пациентов с ХОБЛ и АГ (табл. 2).
При оценке показателей суточной пульсоксиметрии достоверной динамики на фоне лечения Нортиваном® не выявлено.
Не было отмечено существенного влияния Нортивана® на концентрацию общего холестерина, триглицеридов, глюкозы натощак и мочевой кислоты в сыворотке крови.
В 97% случаев у больных ХОБЛ было выявлено увеличение толщины КИМ, у 25,6% отмечено увеличение толщины КИМ на фоне нормального уровня липидного спектра, у 35,7% больных обнаружены в сонных артериях атеросклеротические бляшки различной локализации. В дальнейшем на фоне проводимой терапии статистически значимой динамики не отмечалось.
Клинический пример
Больной А., 58 лет.
Диагноз: хроническая обструктивная болезнь легких III ст., вне обострения. Артериальная гипертензия II ст., риск 4. Цереброваскулярная болезнь: стеноз левой внутренней сонной артерии 42%. Дислипидемия II А типа.
Жалобы: на одышку смешанного характера при ходьбе, кашель со слизистой мокротой в утренние часы, головные боли в затылочной области, эпизодически беспокоят «мушки перед глазами», слабость.
Анамнез: курит с 20 лет по 1,5 пачки в день. Работает слесарем. Хронический кашель много лет. Одышка беспокоит с 2008 года с затрудненным выдохом, которая в дальнейшем стала носить смешанный характер. В июле 2008 г. перенес пневмонию в средней доле правого легкого, в том же году была диагностирована ХОБЛ II ст. Обострения 2-3 раза в год. В течение 3-4 лет отмечает повышение АД, максимальные цифры 175/95 мм рт. ст., адаптирован к 130-140/80-90 мм рт. ст. Постоянного лечения не получал, эпизодически принимал метопролол 50 мг утром. Не обследовался, к врачам не обращался. Базисная терапия ХОБЛ: Беродуал нерегулярно.
Объективный статус: состояние относительно удовлетворительное. Кожные покровы нормальной окраски, умеренной влажности, периферических отеков нет. При перкуссии над легкими коробочный звук, при аускультации везикулярное дыхание, проводящееся во все отделы, единичные дискантовые хрипы. ЧДД 19 в мин. Границы сердца не расширены. Верхушечный толчок в V межреберье по среднеключичной линии. Тоны сердца ясные, ритмичные. АД 170/100 мм рт. ст. ЧСС 90 уд./мин. Язык чистый, влажный. Живот мягкий, безболезненный. Печень не увеличена. Физиологические отправления в норме.
ЭКГ: синусовый ритм. ЧСС 93 уд./мин. Нормальное положение электрической оси сердца. Гипертрофия левого желудочка. Нарушение внутрижелудочковой проводимости.
Результаты терапии: начальная дозировка Нортивана® составила 80 мг/сут. Через 2 недели после анализа индивидуального дневника АД пациента доза была увеличена до 160 мг/сут из-за недостаточного гипотензивного эффекта препарата.
На фоне терапии больной субъективно отметил улучшение самочувствия: уменьшилась слабость, головные боли в затылочной области не беспокоили, эпизоды «мушек перед глазами» не возникали, субъективно несколько уменьшилась выраженность одышки. После 6-месячной терапии Нортиваном® в суточной дозе 160 мг по результатам офисного измерения АД зарегистрирован хороший клинический эффект (АД 130/80 мм рт. ст.). Побочных эффектов не отмечалось.
При контрольном СМАД на фоне терапии отмечалось снижение СрСАД и СрДАД на 13,2% и 18,4% соответственно, уменьшение ВарСАД, показателей нагрузки давлением, улучшение суточного профиля АД (переход из типа non-dipper в dipper) (табл. 3).
При исследовании ФВД было выявлено значительное снижение вентиляционной способности легких по обструктивному типу. Резкая обструкция бронхов на всех уровнях. ЖЕЛ, ФЖЕЛ в норме. ЖЕЛ 92%, ФЖЕЛ 89%, ОФВ 1 55%, индекс Тиффно 49%. В дальнейшем при контрольном исследовании без существенной динамики: ЖЕЛ 89%, ФЖЕЛ 95%, ОФВ 1 56%, индекс Тиффно 47%.
Пульсоксиметрия: распределение SpO 2 (насыщение кислорода): среднее — 95,2%, min — 95%, max — 96%. Эпизоды SpO2 < 89% — 0.Δ Index (12S) — 0. Длительность десатурации: общие события десатурации — 0. Распределение ЧСС: среднее — 96,3 в мин, min — 93%, max — 97%. В дальнейшем при оценке суточной пульсоксиметрии существенной динамики на фоне лечения Нортиваном® не выявлено: распределение SpO 2 (насыщение кислорода): среднее — 96%, min — 95%, max — 97%. Эпизоды SpO 2 < 89% — 0. Δ Index (12S) — 0. Длительность десатурации: общие события десатурации — 0. Распределение ЧСС: среднее — 92 в мин, min — 90%, max — 94%.
Ультразвуковая допплерография: в области бифуркации общей сонной артерии отмечается утолщение КИМ до 1,5 мм справа, 1,0 мм слева. Утолщение КИМ 1 см до бифуркации сонной артерии: слева по передней стенке до 1,1 мм, по задней стенке 0,8 мм; справа до 1,0 мм. Внутренняя сонная артерия слева: КИМ 1,5 мм, стеноз 42%. В дальнейшем при контрольном исследовании без динамики.
Показатели биохимического и клинического анализа крови в процессе терапии без динамики.
Таким образом, данный клинический пример иллюстрирует высокую антигипертензивную эффективность и безопасность Нортивана® у больного АГ очень высокой степени риска в сочетании с ХОБЛ.
Заключение
Применение препарата Нортиван® показало высокую эффективность и безопасность у больных АГ I-II степени в сочетании с ХОБЛ II-IV стадии. Выявлена статистически и клинически значимая нормализация показателей СМАД с коррекцией патологических типов суточных кривых за счет уменьшения количества пациентов с повышением или отсутствием снижения АД в ночной период. Безопасность использования препарата в клинической группе с синдромом бронхообструкции подтверждена динамикой вентиляционных показателей по данным спирометрии и результатами суточной пульсоксиметрии, которые показали отсутствие усугубления гипоксии на фоне терапии.
Литература
- Hurd S. S., Lenfant C. COPD: good lung health is the key. Comment // Lancet. 2005; 366: 1832-1834.
- WHO Key Facts COPD: http://www.who.int/mediacentre/factsheets/fs315/en/index.html .
- Crisafulli E., Costi S., Luppi F. et al. Role of comorbidities in a cohort of patients with COPD undergoing pulmonary rehabilitation // Thorax. 2008; 63: 487-492.
- Мухарлямов Н. М. Легочное сердце. М.: Медицина, 1973, 263 с.
- Мухарлямов Н. М., Саттбеков Ж. С., Сучков В. В. Системная артериальная гипертензия у больных хроническими неспецифическими заболеваниями легких // Кардиология. 1974; № 12 (34): с. 55-61.
- Жданов В. Ф. Клинико-статистическая характеристика больных неспецифическими заболеваниями легких с системной артериальной гипертензией. В кн.: Актуальные проблемы пульмонологии. Сб. науч. тр., Л., 1991; 89-93.
- Задионченко В. С., Погонченкова И. В., Адашева Т. В. Артериальная гипертония при хронической обструктивной болезни легких. Монография. М.: Анахарсис, 2005: 243.
- Задионченко В. С., Адашева Т. В. Глава «Артериальная гипертония у больных хронической обструктивной болезнью легких». Рук-во по артериальной гипертонии под ред. акад. Е. И. Чазова, проф. И. Е. Чазовой. М.: Медиа Медика, 2005: 454-471.
- Задионченко В. С., Адашева Т. В., Федорова И. В., Нестеренко О. И., Миронова М. А. Артериальная гипертония и хроническая обструктивная болезнь легких — клинико-патогенетические параллели и возможности терапии // Российский кардиологический журнал. 2009; 6: 62-69.
- Адашева Т. В., Федорова И. В., Задионченко В. С., Мациевич М. В., Павлов С. В., Ли В. В., Гринева З. О. Клинико-функциональные характеристики артериальной гипертонии у больных хронической обструктивной болезнью легких // Сердце. 2009; 6: 345-351.
- Задионченко В. С., Адашева Т. В., Мациевич М. В. Артериальная гипертония и хроническая обструктивная болезнь легких. Набор слайдов с комментариями. М., 2009: 40.
- Mancia G., De Backer G., Dominiczak A. et al. Guidelines for the Management of Arterial Hypertension. The Task Force for the Management of Arterial Hypertension of the European Society of Hypertension (ESH) and of the European Society of Cardiology (ESC) // J Hypertens. 2007; 25: 1105-1187.
- Диагностика и лечение артериальной гипертензии. Рекомендации Российского медицинского общества по артериальной гипертонии и Всероссийского научного общества кардиологов, 2010. www.gypertonic.ru .
- Hunninghake D. B. Cardiovascular Disease in Chronic Obstructive Pulmonary Disease The Proceedings of the American Thoracic Society. 2005; 2: 44-49.
- Ulfendahl H. R., Aurell M. Renin-Angiotensin. London: Portland Press. 1998; 305.
- Zimmerman B. G., Sybertz E. J., Wong P. C. Interaction between sympathetic and renin-angiotensin system // J Hypertens. 1984; 2: 581-587.
- Goldszer R. C., Lilly L. S., Solomon H. S. Prevalence of cough during angiotensin converting enzyme inhibitor therapy // Am J Med. 1988; 85: 887.
- Lacourciere Y., Lefebvre J., Nakhle G. et al. Association between cough and angiotensin converting enzyme inhibitors vs angiotensin II antagonists: the design of a prospective, controlled study // J Hypertens. 1994; 12: 49-53.
- Chan P., Tomlinson B., Huang T. Y. et al. Double-blind comparison of losartan, lisinopril, and metolazone in elderly hypertensive patients with previous angiotensin-converting enzyme inhibitorinduced cough // J Clin Pharmacol. 1997; 37: 253-257.
- Myou S., Fujimura M., Kamio Y. et al. Effect of losartan, a type 1 angiotensin II receptor antagonist, on bronchial hyperresponsiveness to methacholine in patients with bronchial asthma // Am J Respir Crit Care Med. 2000; 162: 40-44.
В. С. Задионченко*,
Т. В. Адашева*,
доктор медицинских наук, профессор
В. В. Ли*,
кандидат медицинских наук, доцент
Е. И. Жердева*
Ю. В. Малиничева*
О. И. Нестеренко**,
кандидат медицинских наук
С. В. Павлов*
*ГБОУ ВПО МГМСУ Минздравсоцразвития России,
**ГБУЗ ГКБ № 11 Департамента здравоохранения города,
Москва
Национальные клинические рекомендации ВНОК Диагностика и лечение хронической сердечной недостаточности, третий пересмотр (приняты и опубликованы) Диагностика и лечение сердечно-сосудистых заболеваний при беременности (приняты и опубликованы) Диагностика и лечение артериальной гипертензии, четвертый пересмотр (приняты, рекомендованы к публикации) Профилактика сердечно-сосудистых заболеваний (приняты, рекомендованы к публикации)




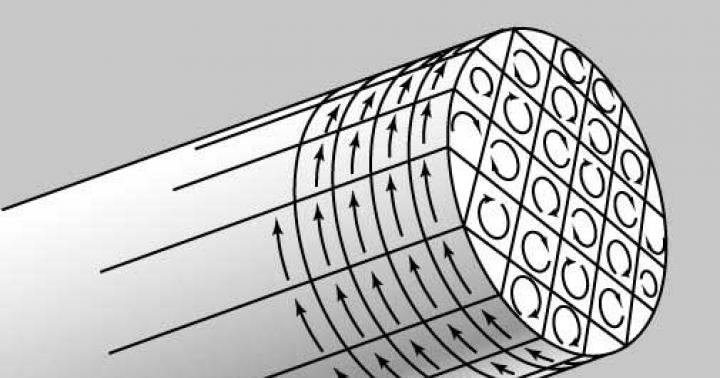
Препараты для лечения ХСН ОСНОВНЫЕ Их эффект на клинику, КЖ и прогноз доказан и сомнений не вызывает 1. ИАПФ 2. БАБ 3. Ант. Альдостер. 4. Диуретики. 5. Дигоксин 6. АРА ДОПОЛНИТЕЛЬНЫЕ Эффективность и без- опасность исследованы, но требуют уточнения ВСПОМОГАТЕЛЬНЫЕ Влияние на прогноз неизвестно, применение диктуется клиникой 1. Статины 2. Антикоагулянты 1.ПВД 2.БМКК 3. Амиодарон 4. Аспирин 5. Негликозид. инотропные А B C


Адреноблокаторы при ХСН Бисопролол Метопролол сукцинат Карведилол Небиволол* В обычных клинических ситуациях только «сверху», при выраженной тахикардии исключение для бисопролола (В) Применение атенолола и метопролола тартрата (!) при ХСН противопоказано


ЦИТОПРОТЕКТОРЫ ПРИ ЛЕЧЕНИИ ХСН ТВЕРДЫХ ДОКАЗАТЕЛЬСТВ НЕТ ИССЛЕДОВАНИЯ ПРОДОЛЖАЮТСЯ Триметазидин может назначаться Триметазидин МОЖЕТ НАЗНАЧАТЬСЯ ТОЛЬКО ДОПОЛНИТЕЛЬНО К ОСНОВНЫМ СРЕДСТВАМ ЛЕЧЕНИЯ ХСН! ИСПОЛЬЗОВАНИЕ ТАУРИНА, КАРНИТИНА, КОЭНЗИМА Q 10, МИЛДРОНАТА В ЛЕЧЕНИИ ХСН НЕ ПОКАЗАНО! ВНОК, 2010


Целевой уровень АД


Артериальная гипертония (АГ), будучи одним из основных независимых факторов риска развития инсульта и ишемической болезни сердца (ИБС), а также сердечно-сосудистых осложнений - инфаркта миокарда (ИМ) и сердечной недостаточности, - относится к чрезвычайно важным проблемам здравоохранения большинства стран мира. Для успешной борьбы с таким распространенным и опасным заболеванием необходима хорошо продуманная и организованная программа по выявлению и лечению. Такой программой безусловно стали рекомендации по АГ, которые регулярно, по мере появления новых данных, пересматриваются . Со времени выхода в 2008 г. третьей версии Российских рекомендаций по профилактике, диагностике и лечению АГ были получены новые данные, требующие пересмотра этого документа . В связи с этим по инициативе Российского медицинского общества по АГ (РМОАГ) и Всероссийского научного общества кардиологов (ВНОК) недавно была разработана новая, четвертая версия этого важнейшего документа, которая прошла детальное обсуждение и в сентябре 2010 г. представлена на ежегодном Конгрессе ВНОК .
В основу настоящего документа легли рекомендации по лечению АГ Европейского общества по артериальной гипертонии (ЕОГ) и Европейского общества кардиологов (ЕОК) 2007 и 2009 гг. и результаты крупных Российских исследований по проблеме АГ. Так же как и в предшествующих версиях рекомендаций, величина АД рассматривается как один из элементов системы стратификации общего (суммарного) сердечно-сосудистого риска. При оценке общего сердечно-сосудистого риска учитывается большое количество переменных, но величина АД является определяющей в силу своей высокой прогностической значимости. При этом уровень АД является наиболее регулируемой переменной в системе стратификации. Как показывает опыт, эффективность действий врача при лечении каждого конкретного пациента и достижение успехов по контролю АД среди населения страны в целом в значительной степени зависят от согласованности действий и терапевтов, и кардиологов, что обеспечивается единым диагностическим и лечебным подходом. Именно эта задача рассматривалась в качестве основной при подготовке рекомендаций.
Целевой уровень АД
Интенсивность лечения больного АГ во многом определяется поставленной целью в плане снижения и достижения определенного уровня АД. При лечении больных АГ величина АД должна быть менее 140/90 мм рт.ст., что является ее целевым уровнем. При хорошей переносимости назначенной терапии целесообразно снижение АД до более низких значений. У пациентов с высоким и очень высоким риском сердечно-сосудистых осложнений необходимо снизить АД до 140/90 мм рт.ст. и менее в течение 4 нед. В дальнейшем, при условии хорошей переносимости рекомендуется снижение АД до 130-139/80-89 мм рт.ст. При проведении антигипертензивной терапии следует иметь в виду, что бывает трудно достичь уровня систолического АД менее 140 мм рт.ст. у пациентов, больных сахарным диабетом, поражением органов-мишеней, у пожилых больных и уже имеющих сердечно-сосудистые осложнения. Дости-жение более низкого целевого уровня АД возможно только при хорошей переносимости и может занимать больше времени, чем его снижение до величины менее 140/90 мм рт.ст. При плохой переносимости снижения АД рекомендуется его снижение в несколько этапов. На каждой ступени АД снижается на 10-15% от исходного уровня за 2-4 нед. с последующим перерывом для адаптации пациента к более низким величинам АД. Следующий этап снижения АД и, соответственно, усиление антигипертензивной терапии в виде увеличения доз или количества принимаемых препаратов возможно только при условии хорошей переносимости уже достигнутых величин АД. Если переход на следующий этап вызывает ухудшение состояния пациента, целесообразно вернуться на предыдущий уровень еще на некоторое время. Таким образом, снижение АД до целевого уровня происходит в несколько этапов, число которых индивидуально и зависит как от исходного уровня АД, так и от переносимости антигипертензивной терапии. Использование этапной схемы снижения АД с учетом индивидуальной переносимости, особенно у пациентов с высоким и очень высоким риском осложнений, позволяет достичь целевого уровня АД и избежать эпизодов гипотонии, с которыми связано увеличение риска развития ИМ и мозгового инсульта. При достижении целевого уровня АД необходимо учитывать нижнюю границу снижения систолического АД до 110-115 мм рт.ст. и диастолического АД до 70-75 мм рт.ст., а также следить за тем, чтобы в процессе лечения не происходило увеличения пульсового АД у пожилых пациентов, что возникает главным образом за счет снижения диастолического АД.
Эксперты все классы антигипертензивных препаратов разделили на основные и дополнительные (табл. 1). В рекомендациях отмечается, что все основные классы антигипертензивных препаратов (ингибиторы АПФ, блокаторы ангиотензиновых рецепторов, диуретики, антагонисты кальция, b-блокаторы) одинаково снижают АД; у каждого препарата есть доказанные эффекты и свои противопоказания в определенных клинических ситуациях; у большинства пациентов с АГ эффективный контроль АД может быть достигнут только при комбинированной терапии, а у 15-20% больных контроль АД не может быть достигнут двухкомпонентной комбинацией; предпочтительны к назначению фиксированные комбинации антигипертензивных препаратов.
Недостатки ведения больных АГ обычно ассоциируются с недостаточным лечением из-за неправильного выбора препарата или дозы, отсутствия синергизма действия при использовании комбинации препаратов и проблем, связанных с приверженностью лечению. По-казано, что комбинации препаратов всегда имеют преимущества в сравнении с монотерапией в снижении АД.
Назначение комбинаций антигипертензивных препаратов может решить все эти проблемы, и поэтому их применение рекомендуется авторитетными экспертами в плане оптимизации лечения АГ. В последнее время было показано, что некоторые комбинации препаратов не только имеют преимущества в осуществлении контроля за уровнем АД, но и улучшают прогноз у лиц с установленной АГ, которая сочетается с другими заболеваниями или нет. Поскольку у врача имеется огромный выбор различных антигипертензивных комбинаций (табл. 2.), то основная проблема состоит в выборе наилучшей комбинации с наибольшими доказательствами для оптимального лечения больных АГ.
В разделе «Медикаментозная терапия» подчеркивается, что у всех больных АГ необходимо добиваться постепенного снижения АД до целевых уровней. Особенно осторожно следует снижать АД у пожилых и у больных, перенесших ИМ и мозговой инсульт. Коли-чество назначаемых препаратов зависит от исходного уровня АД и сопутствующих заболеваний. Например, при АГ 1-й степени и отсутствии высокого риска осложнений возможно достижение целевого АД на фоне монотерапии примерно у 50% больных. При АГ 2-й и 3-й степени и наличии факторов высокого риска в большинстве случаев может потребоваться комбинация из двух или трех препаратов. В настоящее время возможно использование двух стратегий стартовой терапии АГ: монотерапии и низкодозовой комбинированной терапии с последующим увеличением количества и/или доз лекарственного средства при необходимости (схема 1). Монотерапия на старте лечения может быть выбрана для пациентов с низким или средним риском. Комбинация двух препаратов в низких дозах должна быть предпочтительна у больных с высоким или очень высоким риском осложнений. Монотерапия базируется на поиске оптимального для больного препарата; переход на комбинированную терапию целесообразен только в случае отсутствия эффекта последней. Низко-до-зовая комбинированная терапия на старте лечения предусматривает подбор эффективной комбинации препаратов с различными механизмами действия.
Каждый из этих подходов имеет свои преимущества и недостатки. Преимущество низкодозовой монотерапии состоит в том, что в случае удачного подбора лекарства больной не будет принимать еще один препарат. Однако стратегия монотерапии требует от врача кропотливого поиска оптимального для больного антигипертензивного средства с частой сменой лекарств и их дозировок, что лишает врача и больного уверенности в успехе и в конечном счете ведет к снижению приверженности пациентов к лечению. Это особенно актуально для больных АГ 1-й и 2-й степени, большинство из которых не испытывают дискомфорта от повышения АД и не мотивированы к лечению.
При комбинированной терапии в большинстве случаев назначение препаратов с различными механизмами действия позволяет, с одной стороны, добиться целевого АД, а с другой - минимизировать количество побочных эффектов. Комбинированная терапия позволяет также подавить контррегуляторные механизмы повышения АД. Применение фиксированных комбинаций антигипертензивных препаратов в одной таблетке повышает приверженность больных к лечению. Пациен-там с АД≥
160/100 мм рт.ст., имеющим высокий и очень высокий риск, полнодозовая комбинированная терапия может быть назначена на старте лечения. У 15-20% пациентов контроль АД не может быть достигнут при использовании двух препаратов. В этом случае используется комбинация из трех и более лекарственных средств.
Как уже отмечалось ранее, наряду с монотерапией для контроля АД используются комбинации из двух, трех и более антигипертензивных препаратов. Комби-нированная терапия имеет много преимуществ: усиление антигипертензивного эффекта за счет разнонаправленного действия препаратов на патогенетические механизмы развития АГ, что увеличивает число пациентов со стабильным снижением АД; уменьшение частоты возникновения побочных эффектов, как за счет меньших доз комбинируемых антигипертензивных препаратов, так и за счет взаимной нейтрализации этих эффектов; обеспечение наиболее эффективной органопротекции и уменьшение риска и числа сердечно-сосудистых осложнений. Однако необходимо помнить, что комбинированная терапия - это прием как минимум двух лекарственных препаратов, кратность назначения которых может быть различной. Следовательно, применение препаратов в виде комбинированной терапии должно отвечать следующим условиям: препараты должны иметь взаимодополняющее действие; должно достигаться улучшение результата при их совместном применении; препараты должны иметь близкие фармакодинамические и фармакокинетические показатели, что особенно важно для фиксированных комбинаций.
Приоритет рациональных комбинаций антигипертензивных препаратов
Эксперты РМОАГ предлагают разделить комбинации двух антигипертензивных препаратов на рациональные (эффективные), возможные и нерациональные. Американские эксперты, которые в 2010 г. представили новый алгоритм комбинированной антигипертензивной терапии (табл. 3), занимают в этом вопросе практически такие же позиции . Эта позиция полностью совпадает с мнением европейских экспертов по АГ, высказанным в ноябре 2009 г. по вопросам комбинированной терапии и представленным на рисунке 1.
В Российских рекомендациях подчеркивается, что в полной мере преимущества комбинированной терапии присущи только рациональным комбинациям антигипертензивных препаратов (табл. 2). Среди многих рациональных комбинаций за-служивают особого внимания некоторые, имеющие преимущества не только с теоретических позиций ос-новного механизма действия, но и практически доказанной высокой антигипертензивной эффективности. В первую очередь эта комбинация ингибитора АПФ с диуретиком, при которой усиливаются преимущества и нивелируются недостатки. Данная комбинация является наиболее популярной в терапии АГ благодаря высокой гипотензивной эффективности, защите органов-мишеней, хорошей безопасности и переносимости. В опубликованных рекомендациях Американского общества АГ (ASH) по комбинированной терапии АГ (табл. 3) также приоритет (более предпочтительные) отдается комбинации препаратов, блокирующих активность ренин-ангиотензиновой системы (блокаторы ангиотензиновых рецепторов или ингибиторы АПФ) с диуретиками или с антагонистами кальция .
Препараты потенцируют действие друг друга за счет взаимодополняющего влияния на основные звенья регуляции АД и блокады контррегуляторных механизмов. Снижение объема циркулирующей жидкости вследствие салуретического действия диуретиков приводит к стимуляции ренинa:2:{s:4:"TEXT";s:65522:"-ангиотензиновой системы (РАС), чему противодействует ингибитор АПФ. У пациентов с низкой активностью ренина плазмы ингибиторы АПФ обычно недостаточно эффективны, и добавление диуретика, приводящего к повышению активности РАС, позволяет ингибитору АПФ реализовать свое действие. Это расширяет круг больных, отвечающих на терапию, и целевые уровни АД достигаются более чем у 80% пациентов. Ингибиторы АПФ предотвращают гипокалиемию и уменьшают негативное влияние диуретиков на углеводный, липидный и пуриновый обмен.
Ингибиторы АПФ широко используются в лечении больных АГ, острых форм ИБС, хронической сердечной недостаточности. Один из представителей большой группы ингибиторов АПФ - лизиноприл. Препарат был детально изучен в нескольких крупномасштабных клинических исследованиях. Лизиноприл продемонстрировал профилактическую и терапевтическую эффективность при сердечной недостаточности, в том числе после острого ИМ, и при сопутствующем сахарном диабете (исследования GISSI 3, ATLAS, CALM, IMPRESS). В самом крупном клиническом исследовании по лечению АГ различными классами препаратов ALLHAT среди принимавших лизиноприл достоверно снизилась заболеваемость СД 2-го типа .
В российском фармакоэпидемиологическом исследовании ПИФАГОР III изучались предпочтения практических врачей в выборе антигипертензивной терапии. Результаты были сопоставлены с предшествующим этапом исследования ПИФАГОР I в 2002 г. . По данным этого опроса врачей, структура антигипертензивных препаратов, которые назначаются пациентам с АГ в реальной практике, представлена пятью основными классами: ингибиторами АПФ (25%), β
-адреноблокаторами (23%), диуретиками (22%), антагонистами кальция (18%) и блокаторами ангиотензиновых рецепторов. В сравнении с результатами исследования ПИФАГОР I наблюдается уменьшение доли ингибиторов АПФ на 22% и β
-блокаторов на 16%, увеличение доли антагонистов кальция на 20% и почти 5-кратное увеличение доли блокаторов рецепторов ангиотензина II.
В структуре препаратов класса ингибиторов АПФ наибольшие доли имеют эналаприл (21%), лизиноприл (19%), периндоприл (17%), фозиноприл (15%) и рамиприл (10%). Вместе с тем в последние годы наблюдается тенденция к повышению значимости и частоты применения комбинированной антигипертензивной терапии для достижения целевого уровня у пациентов с АГ. По данным исследования ПИФАГОР III в сравнении с 2002 г. подавляющее большинство (около 70%) врачей предпочитают использовать комбинированную терапию в виде свободных (69%), фиксированных (43%) и низкодозовых комбинаций (29%) и только 28% продолжают применять тактику монотерапии. Среди комбинаций антигипертензивных препаратов 90% врачей предпочитают назначение ингибиторов АПФ с диуретиком, 52% - β
-блокаторов с диуретиком, 50% врачей назначают не содержащие диуретики комбинации (антагонисты кальция с ингибиторами АПФ или